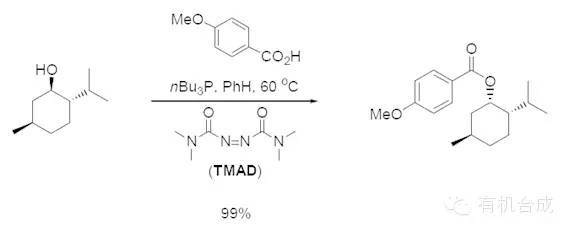
mitsunobu反应(光延反应)是一种双分子亲核取代反应(sn2反应)。1967年, mitsunobu 报导了在三膦(pph3)和偶氮二甲酸二乙酯(dead)作用下酸和醇缩合成酯的新方法。当底物为仲醇的时候,与羟基相连的碳原子的构型会发生翻转。经过多年的研究和发展,形成了一大类合成方法,我们称之为mitsunobu 反应。这类反应被广泛应用在有机合成,特别是天然产物的合成中。其反应可表示为:
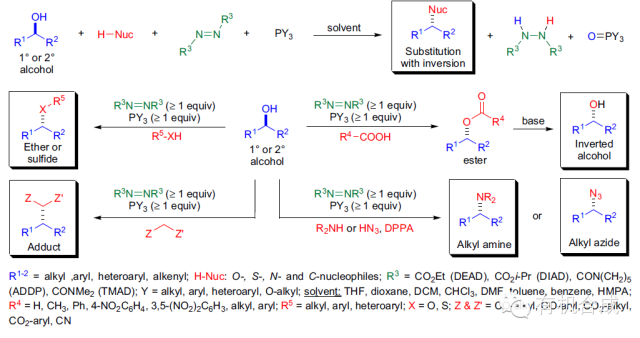
反应机理:
mitsunobu反应机理相当复杂,其中的中间体实体以及它们所起的作用仍然有许多争论。
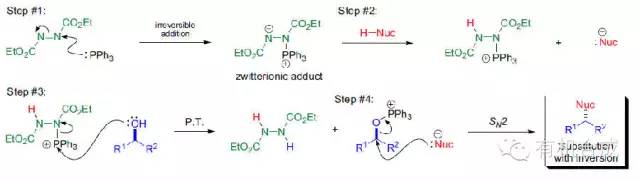
先是三基膦进攻dead形成中间体,夺取羧酸质子形成正离子,亲核试剂进攻离子的膦正中心形成氧膦离子,而dead脱落下来形成肼的副产物。虽然说反应当中参与了很多的膦中间体,但是step4是唯一形成产物的路径并且后得到三基氧膦副产物。
反应特点:
一、伯醇和仲醇可以进行mitsunobu反应,仲醇手性翻转,叔醇不反应;二、亲核试剂质子的pka值必须小于甜菜碱式中间体(betaineintermediate)的pka 值(~13),否则亲核试剂的质子不能被中间体夺取;三、氧亲核试剂主要产物为酯和醚,硫亲核试剂主要得到硫醚,氮亲核试剂常见的有酰亚胺,羟胺,杂环氮和叠氮酸;四、也可以生成碳碳键,亲核试剂主要是活性亚甲基化合物,如β-二酮,β-酮酸酯等等,但β-二酯活性达不到;五、可以进行分子内反应,三元、四元、五元、六元和七元环醚和环胺可以用此反应制备;六、用酰卤,卤化锌或卤化锂作为卤离子源,可以把醇转化为相应的卤化物;七、低极性的溶剂有利于反应,通常用四氢呋喃,,二氯甲烷和作为溶剂,有时候,乙腈和dmf也用作溶剂;八、pph3和 p(n-bu)3是常用的膦配体,常用的偶氮二羧酸酯是dead 和 diad,反应中此两种试剂可以互换;九、反应温度通常在0℃到25℃之间,底物的位阻较大的反应温度也要提高;十、投料顺序至关重要,首先应当将亲核试剂,底物,三基膦溶解于适当的溶剂当中,比如四氢呋喃(或者等),冷至零度,然后将dead缓慢滴加,后在室温下搅拌。若反应不完可以升温到室温或者继续加热进行。另外一种投料方式,是将三基膦和dead先于溶剂中搅拌,再将底物和亲核试剂依次溶剂加入。
醇的翻转
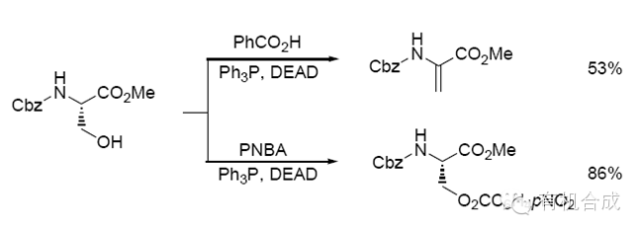
用p-硝基甲酸(pnba)作为亲核试剂对立体位阻较大的醇的翻转更有效,p-硝基甲酸(pnba)还能有效地抑制副反应:醇的消除。所以,在mitsunobu反应中,通常使用p-硝基甲酸(pnba)作为亲核试剂。
tsunoda等发现,对于位阻较大的醇,tmad(n, n, n’, n’-tetramethyl-azodicarboxamide) 和三丁基膦的体系效果比较好。